| |
XVII Congresso Nazionale Associazione Medici Diabetologi
Certezze ed incertezze sull'autocontrollo della glicemia
nel diabete di tipo 2
Rimini, 28 maggio 2009 – Sull’importanza educativa e terapeutica dell’automonitoraggio glicemico (SMBG, self monitoring of blood glucose) nel diabete insulinotrattato (specie quello di tipo 1) esistono certezze assolute; più dubbio è il ruolo nel diabete di tipo 2. È stato questo l’oggetto di una sessione parallela moderata da Rossella Iannarelli (L’Aquila) e Claudio Noacco (Udine).

A. Nicolucci |
|
Il primo intervento, dedicato alla difficoltà nel disegnare i trial, è stato quello di Antonio Nicolucci (Consorzio Mario Negri Sud; Santa Maria Imbaro, Chieti). I risultati della letteratura disponibile sono poco confortanti, parlando di una riduzione dei livelli di emoglobina glicata (HbA1c) ai limiti della significatività statistica, e compresa tra lo 0,2-0,3%, nei soggetti in sola dieta o in terapia antidiabetica orale. La maggior parte degli studi è tuttavia viziata da problemi metodologici che limitano le possibilità d’interpretarne i risultati, sia in termini di validità sia di generalizzabilità. Un difetto comune, negli studi sull’efficacia dell’SMBG nel migliorare il compenso glicemico, è quello di non fornire ai pazienti un modello educativo strutturato o degli algoritmi utili a modificare i comportamenti (farmacologici, dietetici o di attività fisica) sulla base delle glicemie rilevate, limitandosi alla semplice registrazione dei valori. Molto spesso, inoltre, gli studi sono gravati da limiti di aderenza dei pazienti: se la frequenza dell’SMBG è troppo elevata, il tasso di drop-out può risultare talmente rilevante da diluire l’effetto reale dell’intervento, giacché l’analisi dei risultati viene effettuata secondo il principio intent-to-treat (che tiene conto dei dati relativi a tutti i soggetti arruolati, indipendentemente dal fatto che abbiano portato a termine lo studio o meno); se è troppo bassa, l’impatto dell’intervento potrà risultare scarso. Anche la selezione dei soggetti può nascondere delle insidie: scegliendo individui che praticavano l’SMBG sporadicamente potremmo selezionare persone poco motivate; se già lo effettuavano in maniera intensiva, potranno rimanere delusi dall’eventuale allocazione nel gruppo di controllo.

Figura 1
|

Figura 2 |
Nicolucci ha quindi spiegato come i benefici dimostrabili varino in relazione ai livelli di HbA1c di partenza e del tipo di terapia in atto: gli studi che hanno dimostrato la massima efficacia dell’SMBG partivano da livelli elevati di emoglobina glicata. In realtà, la fascia di popolazione in terapia antidiabetica orale ha per lo più valori di HbA1c <8%, e tale fattore limita i risultati obiettivabili. È stato poi rimarcato come sia difficile distinguere se i benefici dipendano dall’intervento (l’automonitoraggio) o dall’educazione fornita di per sé. Il problema concettuale più importante, secondo il relatore, è la necessità di definire, negli obiettivi dello studio, a cosa serva l’SMBG, oltre a influenzare gli indici di compenso: ad aiutare il paziente a modificare il proprio stile di vita? A correggere la terapia? Oppure a ridurre l’inerzia terapeutica del medico? Anche l’endpoint va scelto in maniera opportuna, non dovendo essere obbligatoriamente l’HbA1c (Figura 1): nei soggetti in buon compenso (es.: HbA1c <7,5%) potrebbe essere più opportuno valutare la variabilità glicemica, gli episodi ipoglicemici, la qualità della vita o le decisioni d’intensificazione terapeutica che ne derivino; per i soggetti in cattivo compenso (HbA1c >9%), invece, il problema non si pone, essendo candidati immediati alla terapia insulinica (Figura 2). Gli studi futuri dovranno essere disegnati prevedendo un periodo di run-in (per escludere i soggetti con compliance minore), una randomizzazione stratificata sulla base dei livelli di emoglobina glicata e un pacchetto educativo standardizzato ai pazienti, oltre a un algoritmo di variazione della terapia sulla base dei risultati dell’SMBG. Necessario, infine, scegliere un campione di dimensioni adeguate e un follow-up sufficiente.

Figura 3 |

Figura 4
|
| |

A. De Micheli |
La sessione è proseguita con l’intervento di Alberto De Micheli (Genova; Consigliere Nazionale AMD), che ha effettuato una dettagliata rassegna delle evidenze disponibili in letteratura. Gli “Standard Italiani per la Cura del Diabete Mellito” (1), in effetti, raccomandano l’SMBG quale componente indispensabile della gestione clinica del soggetto con diabete, ma la forza di tale affermazione è limitata (a seconda delle condizioni, il livello è compreso tra III e VI, con una forza di tipo B o C) (Figura 3 e Figura 4). Analizzando la letteratura sul ruolo dell’SMBG nel migliorare il compenso glicemico (2), s’incontrano studi non sperimentali (trasversali, di coorte) (3-6), sperimentali (RCT) e pseudo-sperimentali (con interventi di tipo diverso) (7-11), e metanalisi (12-18). In molti casi, i risultati che emergono mostrano un vantaggio in termini di HbA1c di pochi decimi percentuali, che riguarda soprattutto soggetti con un compenso basale mediocre (Figura 5). Se tale riduzione risulta significativa dal punto di vista statistico, una classica obiezione è se lo sia anche dal punto di vista clinico; De Micheli ha provato a effettuare una stima deduttiva, basata sull’analisi dei risultati dell’UKPDS, secondo la quale tale variazione potrebbe conferire una riduzione del 7-15% come rischio di complicanze microvascolari e del 2-3% come eventi vascolari maggiori. In alcuni casi, parallelamente all’emergere di un vantaggio di Hba1c (e indipendentemente da esso), è stato documentato un beneficio in termini di stress correlato alla gestione della malattia. Esistono, peraltro, episodiche segnalazioni di autori che hanno rilevato come la restrizione nella dispensazione rimborsata delle strisce non abbia provocato un peggioramento del compenso, anche se (come spesso avviene) tale conclusione si basava unicamente sugli effetti relativi all’HbA1c. È inoltre possibile che i pazienti cui era stata ristretta la fornitura avessero fatto proprie, nel periodo precedente alla limitazione, consuetudini di stili di vita e gestionali atte ad assicurarne comunque risultati migliori.
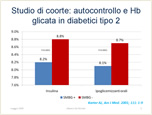
Figura 5
|

Figura 6 |
Anche limitandosi alle variazioni di HbA1c, i risultati della maggior parte delle metanalisi condotte sull’SMBG sembrano documentare un vantaggio, mentre lo stesso non può essere affermato per l’automonitoraggio basato sui dati ricavati dalla glicosuria (12-18) (Figura 6). Sono però pochissimi gli studi che abbiano esaminato i mediatori e i moderatori dell’SMBG sul compenso glicemico, o che abbiano analizzato separatamente l’eventuale intervento attivo di modifica della terapia conseguente alla rilevazione dei risultati dell’SMBG. In realtà, il feed-back dell’automonitoraggio e la capacità d’intervenire sulle terapie paiono fondamentali. Anche sulla durata del vantaggio esistono dati contrastanti: secondo la maggior parte delle pubblicazioni il beneficio sarebbe limitato nel tempo, non protraendosi oltre i 9-12 mesi (quasi “l’entusiasmo” dell’assistito si perdesse con il passare dei mesi). Proprio sulla durata dell’efficacia dell’SMBG dovranno concentrarsi gli sforzi delle ricerche future, allo scopo di valutare se l’intervento possa tradursi anche in una riduzione nell’insorgenza e progressione delle complicanze croniche. Altre analisi dovranno valutare, quali endpoint aggiuntivi, gli effetti sulla diminuzione dei ricoveri ospedalieri, sulla qualità della vita e i reali rapporti costo-beneficio dell’automonitoraggio.

N. Musacchio |
|
L’ultima relazione è stata quella di Nicoletta Musacchio (Milano; Gruppo Percorsi Assistenziali di AMD), incentrata su SMBG ed educazione del paziente. La relatrice ha esordito ricordando con orgoglio il documento intersocietario AMD-SID sulle “Raccomandazioni sull’uso dell’automonitoraggio domiciliare della glicemia”, risalente al 2002. Era già contenuta in tale documento l’affermazione sull’utilità dell’SMBG nello stabilire i target glicemici, fornire raccomandazioni per la terapia, valutarne l'efficacia, istruire il paziente a interpretare e a intervenire secondo i valori glicemici, e identificare le ipoglicemie "silenti". Trattandosi di uno strumento costoso, è opportuno che lo specialista decida quanto si possa investire in tale intervento. Negli ultimi anni, il livello glicemico sta acquisendo nuova dignità propria, affiancandosi a parametri consolidati quali l’HbA1c: si pensi ad esempio al ruolo attribuito all’iperglicemia post-prandiale e alla variabilità glicemica nella genesi delle complicanze cardiovascolari. Il problema reale è quindi non tanto l’autocontrollo, ma come lo utilizziamo.

Figura 7
|

Figura 8 |
Dei moltissimi lavori disponibili, ha ribadito Musacchio, sono esigui quelli di qualità metodologica accettabile. Anche se la dimostrabilità dell’efficacia dell’SMBG è spesso stata messa in discussione, tale strumento possiede rilevanti potenzialità; sono pochi, tuttavia, i pazienti che ricevono il feedback dai curanti sui propri risultati, e ancora meno quelli che lo utilizzano per la rilevazione delle glicemie post-prandiali. Forse, ha detto Musacchio, “non abbiamo ancora chiari gli obiettivi che l’SMBG ci permette di raggiungere”. L’autocontrollo deve essere previsto come strumento terapeutico di comprensione e monitoraggio sia per il paziente sia per il medico (Figura 7 e Figura 8), ma è necessario istruire il paziente, valutare periodicamente la correttezza dell’utilizzo del glucometro e la capacità di modificare la terapia sulla base dei valori misurati, eventualmente facendo uso di algoritmi condivisi (come recitano gli Standard Italiani) (1). Da tempo si sta sottolineando l’importanza dell’evoluzione della nostra pratica professionale verso una medicina centrata sulla persona, ma per raggiungere tale obiettivo serve anche che il soggetto con diabete arrivi ad assumersi e a condividere con il Diabetologo la responsabilità della terapia e del proprio stato di salute. Grazie all’SMBG, il paziente potrà: capire perché sta male e interpretare più correttamente glicemie elevate in assenza di sintomatologia (prendendo coscienza di una reale alterazione da curare); rendersi conto di come procede il controllo; imparare ad “aggiustare il tiro”, patteggiando con il medico tra i suoi bisogni e quelli della cura, sperimentando soluzioni alternative e sentendosi libero di agire; potrà infine acquisire la consapevolezza di essere in grado di governare (seppur guidato) il suo controllo glicemico.
L’SMBG s’inserisce quindi nel percorso di enpowerment del paziente, inteso come “legittimazione”, “assunzione di responsabilità” e “modulazione della propria autonomia”. La relatrice ha infine ribadito come gli studi non considerino le reali condizioni di utilizzo degli strumenti (19), oltre all’istruzione fornita ai pazienti; devono infatti essere questi ultimi i protagonisti nella scelta degli obiettivi, seppur aiutati dai Curanti, nel principio del superamento della “medicina pedagogica”. Una nuova sfida, ha concluso Musacchio, “sarà quella di andare a vagliare l’efficacia dell’autocontrollo scegliendo indicatori coerenti con la natura di strumento PER la cura (e non DI cura), assumendoci la responsabilità della prescrizione, del controllo e dei costi inerenti.
Alla domanda della platea se sia giusto subire le restrizioni imposte dai legislatori nella prescrizione del materiale per l’automonitoraggio, i relatori hanno commentato come sia indispensabile che specialisti e società scientifiche contribuiscano a evitare sprechi, pur nell’ambito delle difficoltà insite nel decidere come regolamentare una prescrizione razionale. Occorre recitare il “mea culpa”, come diabetologi, sul fatto di non essere stati in grado di produrre evidenze inoppugnabili che dimostrassero inequivocabilmente i vantaggi dell’SMBG per la salute del soggetto con diabete, seppure per quella costruita su misura per ciascuno di essi.
Riferimenti bibliografici:
1) Standard italiani per la cura del diabete mellito, Diabete Italia, AMD, SID, 2007
2) St John A e coll., J Diabetes Complications. 2009 Feb 19. [Epub ahead of print]
3) Karter AJ e coll., Am J Med. 2001; 111: 1-9
4) Karter AJ e coll., Diabetes Care 2006; 29: 1757–1763
5) Franciosi M e coll., Diabetes Care 2001; 24: 1870–1877
6) Martin S e coll., Diabetologia 2006; 49: 271−278
7) Barnett AH e coll., Diabetes Obes Metab. 2008; 10: 1239-1247
8) Guerci B e coll., Diabetes Metab. 2003; 29: 587- 594
9) Schwedes U e coll., Diabetes Care 2002; 25 : 1928-1932
10) Farmer A e coll., British Medical Journal 2007; 335: 132−136
11) O’Kane MJ e coll., BMJ 2008; 336; 1174-1177
12) Welschen LM e coll., Cochrane Database of Systematic Reviews 2005, Issue 2. Art. No.: CD005060. DOI: 10.1002/14651858.CD005060.pub2
13) Sarol JN Jr e coll., Curr Med Res Opin 2005; 21: 173-184
14) Jansen JP e coll., Curr Med Res Opin. 2006; 22: 671-681
15) McGeoch G e coll., Diabetes/Metabolism Research and Reviews 2007; 23, 423−440
16) McAndrew L e coll., The Diabetes Educator 2007; 33; 991-1011
17) Towfigh A e coll., Am J Manag Care. 2008; 14: 468-475
18) Poolsup N e coll., Diabetes technology & therapeutics 2008; 10: s51-s66
19) Hirsch IB e coll., Diabetes Technol & Therap 2008, 10(6): 419-439 |
|